[ad_1]
Pada hari Rabu, Badan Pengawas Obat dan Makanan AS diberikan otorisasi penggunaan darurat (EUA) kepada perusahaan biofarmasi global AstraZeneca untuk kombinasi antibodi kerja panjang yang melindungi terhadap COVID-19, ditemukan tahun lalu di Vanderbilt University Medical Center (VUMC). Sejumlah kondisi medis mengakibatkan kompromi kekebalan, dari perawatan untuk banyak kanker hingga transplantasi organ.
Kombinasi dua antibodi monoklonal, yang disebut Evusheld, disahkan sebagai profilaksis pra-pajanan untuk mencegah COVID-19 pada orang dewasa dan anak-anak berusia 12 tahun ke atas yang memiliki sistem kekebalan yang terganggu atau riwayat reaksi merugikan yang parah terhadap vaksin COVID-19.
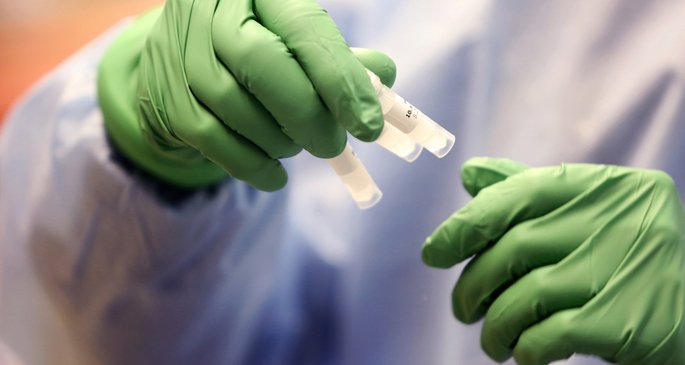
Ilustrasi oleh Erin O. Smith
Kombinasi antibodi ini ditemukan di Vanderbilt Vaccine Center yang disutradarai oleh James Crowe, MD.
“Kami bangga dengan kontribusi Vanderbilt dalam pertempuran melawan COVID-19. Antibodi yang ditemukan oleh tim Dr. Crowe menawarkan perlindungan tambahan bagi jutaan orang dengan gangguan kekebalan yang tidak sepenuhnya dilindungi oleh vaksin dan berisiko terkena infeksi parah selama pandemi,” kata Jeff Balser, MD, PhD, Presiden dan Chief Executive Officer dari VUMC dan Dekan Fakultas Kedokteran Universitas Vanderbilt.
Studi telah menemukan bahwa Evusheld secara efektif mencegah infeksi dari virus COVID-19 pada mereka yang saat ini tidak terinfeksi atau diketahui baru saja terpapar. Dalam uji coba utama yang mendukung EUA FDA, lebih dari 5.000 orang menerima Evusheld atau plasebo.
Penerima evusheld mengalami penurunan risiko 77% terkena COVID-19 dibandingkan dengan mereka yang diobati dengan plasebo, dan pengurangan risiko dipertahankan selama enam bulan. Menurut FDA, tidak ada alternatif yang memadai, disetujui, dan tersedia untuk Evusheld untuk mencegah infeksi COVID-19 pada pasien dengan gangguan sistem kekebalan atau pada pasien dengan riwayat reaksi merugikan yang parah (misalnya, reaksi alergi parah) terhadap vaksin COVID-19.
“Kami sangat senang melihat antibodi ini mendapatkan persetujuan penggunaan darurat, karena mereka akan menjadi satu-satunya antibodi yang diizinkan di AS untuk profilaksis pra-pajanan,” kata Crowe, yang memimpin penelitian di VUMC.
“Tembakan pencegahan ini akan memberi jutaan orang berisiko tinggi dan immunocompromised yang tidak merespon dengan baik akses vaksin ke kekebalan untuk COVID,” kata Crowe.
Antibodi monoklonal lain yang diberikan otorisasi penggunaan darurat (EUA) oleh FDA dikirimkan melalui infus intravena kepada orang yang sudah terinfeksi oleh virus COVID-19 untuk mencegah penyakit parah atau rawat inap.
Berdasarkan AstraZeneca, Evusheld mungkin bermanfaat bagi sekitar 7 juta orang di Amerika Serikat yang mungkin tidak merespon secara memadai terhadap vaksin COVID-19 karena obat yang mereka gunakan untuk mencegah penolakan organ yang ditransplantasikan atau mengobati penyakit termasuk kanker, multiple sclerosis, dan rheumatoid arthritis menekan respons imun mereka.
Temuan laboratorium awal menunjukkan bahwa Evusheld dapat menetralkan varian virus yang muncul baru-baru ini, termasuk varian delta, kata pejabat AstraZeneca. Studi sedang dilakukan untuk menentukan seberapa efektif kombinasi tersebut terhadap varian omicron yang baru muncul.
“Kami semua sedang memeriksa omicron sekarang,” kata Crowe, Profesor Ann Scott Carell dan profesor Pediatri dan Patologi, Mikrobiologi & Imunologi di VUMC. “Saya memperkirakan pendekatan umum ini akan mengubah cara kita berpikir tentang peran keseluruhan antibodi monoklonal dalam pencegahan banyak penyakit menular lainnya.”
Crowe dan rekan-rekannya telah berkembang metode ultra-cepat untuk menemukan antibodi monoklonal manusia antivirus yang sangat kuat dan memvalidasi keefektifannya.
Pada Juni 2020, enam antibodi COVID-19 yang diisolasi di VUMC dilisensikan ke AstraZeneca untuk pengoptimalan dan kemajuan dalam pengembangan klinis. Pada Januari 2021, perusahaan mengumumkan sedang mengembangkan kombinasi dua antibodi kerja panjang ke dalam uji klinis fase 3.
Sumber: Universitas Vanderbilt
[ad_2]